Lista de elementos
»
actinio
»
aluminio
»
americio
»
argón
»
arsénico
»
astato
»
azufre
»
bario
»
Berilio
»
berkelio
»
bismuto
»
bohrio
»
Boro
»
bromo
»
cadmio
»
calcio
»
carbono
»
cerio
»
cesio
»
circonio
»
cloro
»
cobalto
»
cobre
»
conducir
»
criptón
»
cromo
»
curio
»
dubnio
»
erbio
»
escandio
»
estaño
»
europio
»
fermio
»
flúor
»
fósforo
»
francio
»
galio
»
germanio
»
hafnio
»
hassio
»
helio
»
hierro
»
holmio
»
indio
»
iridio
»
iterbio
»
itrio
»
lantano
»
litio
»
lutecio
»
magnesio
»
mercurio
»
neodimio
»
neón
»
neptunio
»
Nihonium
»
niobio
»
níquel
»
nobelio
»
oro
»
osmio
»
oxígeno
»
paladio
»
Plata
»
platino
»
plutonio
»
polonio
»
potasio
»
prometeo
»
radio
»
radón
»
renio
»
rodio
»
rubidio
»
rutenio
»
samario
»
selenio
»
silicio
»
sodio
»
talio
»
tantalio
»
tecnecio
»
telurio
»
Tennesse
»
terbio
»
titanio
»
torio
»
tulio
»
uranio
»
vanadio
»
xenón
»
yodo
»
zinc
Rh - rodio - METAL DE TRANSICIÓN
El rodio es un metal de transición de la familia del platino blanco y es uno de los metales más caros del mundo. Su número atómico es 45 y su símbolo es Rh.
El rodio es un metal blanco plateado que es muy refractario y resistente a la oxidación. Es uno de los metales más duros y brillantes, con una dureza específica de 16,3 (frente a 4,5 del oro y 5,5 del platino).
El rodio es altamente humectable y altamente refractario, lo que lo convierte en el metal óptimo para pulir y enchapar metales preciosos. También es insensible al ácido clorhídrico y no reacciona a los ácidos débiles.
El rodio se utiliza principalmente en aleaciones, revestimientos y aplicaciones industriales. También se utiliza para enchapar joyas y monedas. El rodio también se utiliza como catalizador en los procesos de hidrogenación y es muy eficaz para convertir hidrocarburos en productos más valiosos y volátiles. Finalmente, el rodio también se utiliza como recubrimiento de vidrios para aumentar su resistencia a la corrosión y al calor.
El rodio es un metal blanco plateado que es muy refractario y resistente a la oxidación. Es uno de los metales más duros y brillantes, con una dureza específica de 16,3 (frente a 4,5 del oro y 5,5 del platino).
El rodio es altamente humectable y altamente refractario, lo que lo convierte en el metal óptimo para pulir y enchapar metales preciosos. También es insensible al ácido clorhídrico y no reacciona a los ácidos débiles.
El rodio se utiliza principalmente en aleaciones, revestimientos y aplicaciones industriales. También se utiliza para enchapar joyas y monedas. El rodio también se utiliza como catalizador en los procesos de hidrogenación y es muy eficaz para convertir hidrocarburos en productos más valiosos y volátiles. Finalmente, el rodio también se utiliza como recubrimiento de vidrios para aumentar su resistencia a la corrosión y al calor.
Sintético
Radiactivo
Liquido
Gaseoso
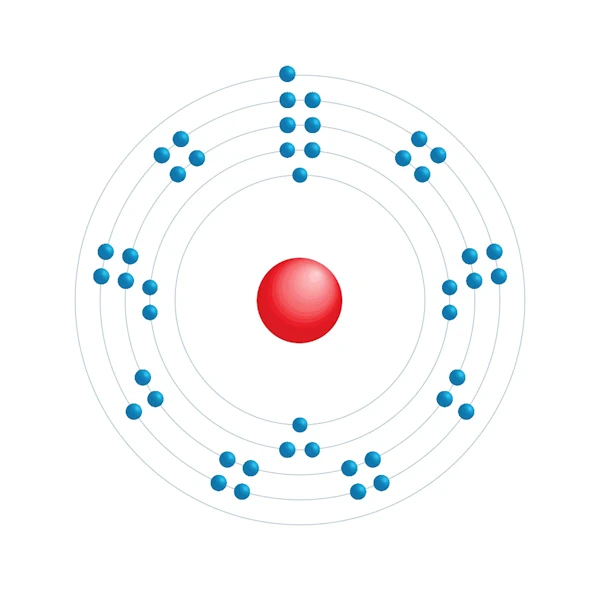
Diagrama de configuración electrónica
| Apellido | rodio |
| Número | 45 |
| Atómico | 102.9055 |
| Símbolo | Rh |
| Fusión | 1966 |
| Hirviendo | 3727 |
| Densidad | 12.41 |
| Período | 5 |
| Grupo | 9 |
| Descubrimiento | 1803 Wollaston |
| Abundancia | 0.001 |
| Radio | 1.8 |
| Electronegatividad | 2.28 |
| Ionización | 7.4589 |
| Número de isótopos | 20 |
| Configuración electrónica | [Kr] 4d8 5s1 |
| Estados de oxidación | -1,1,2,3,4,5,6 |
| Electrón por nivel de energía | 2,8,18,16,1 |
| Mineral | Dureza | Densidad |
| Bowieite | 7.00 / 7.00 | |
| Cherepanovite | 6.00 / 6.00 | 9.72 |
| Cuprorhodsite | 5.00 / 5.50 | 6.74 |
| Ferhodsite | ||
| Ferrorhodsite | 4.50 / 4.50 | 5.71 |
| Hollingworthite | 6.00 / 6.50 | 7.91 |
| Irarsite | 6.50 / 6.50 | 11.00 |
| Kashinite | 7.50 / 7.50 | 9.10 |
| Kingstonite | 6.00 / 6.00 | 7.52 |
| Konderite | 5.50 / 5.50 | 4.73 |
| Miassite | 5.50 / 6.00 | |
| Palladodymite | ||
| Platarsite | 7.50 / 7.50 | 8.00 |
| Polkanovite | 10.22 | |
| Rhodarsenide | 4.00 / 5.00 | 11.27 |
| Rhodium | 3.50 / 3.50 | 16.51 |
| Rhodplumsite | 9.00 | |
| Xingzhongite | 6.00 / 6.00 | 6.64 |
| Zaccariniite | 3.50 / 4.00 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se