Lista de elementos
»
actinio
»
aluminio
»
americio
»
argón
»
arsénico
»
astato
»
azufre
»
bario
»
Berilio
»
berkelio
»
bismuto
»
bohrio
»
Boro
»
bromo
»
cadmio
»
calcio
»
carbono
»
cerio
»
cesio
»
circonio
»
cloro
»
cobalto
»
cobre
»
conducir
»
criptón
»
cromo
»
curio
»
dubnio
»
erbio
»
escandio
»
estaño
»
europio
»
fermio
»
flúor
»
fósforo
»
francio
»
galio
»
germanio
»
hafnio
»
hassio
»
helio
»
hierro
»
holmio
»
indio
»
iridio
»
iterbio
»
itrio
»
lantano
»
litio
»
lutecio
»
magnesio
»
mercurio
»
neodimio
»
neón
»
neptunio
»
Nihonium
»
niobio
»
níquel
»
nobelio
»
oro
»
osmio
»
oxígeno
»
paladio
»
Plata
»
platino
»
plutonio
»
polonio
»
potasio
»
prometeo
»
radio
»
radón
»
renio
»
rodio
»
rubidio
»
rutenio
»
samario
»
selenio
»
silicio
»
sodio
»
talio
»
tantalio
»
tecnecio
»
telurio
»
Tennesse
»
terbio
»
titanio
»
torio
»
tulio
»
uranio
»
vanadio
»
xenón
»
yodo
»
zinc
In - indio - OVERGANGSMETAAL
El indio es un elemento químico metálico que pertenece al grupo 13 y al período 5 de la tabla periódica de elementos. Con símbolo atómico In y número atómico 49, el indio tiene 13 isótopos conocidos, con una masa atómica que varía entre 121 y 133. Tiene un peso atómico relativo de 114,82.
El indio tiene un punto de fusión de 156,60 °C y un punto de ebullición de 2072 °C. Tiene una densidad relativa de 7,29 g/cm3 y un estado de oxidación de +3. Su color es blanco grisáceo cuando está puro, pero toma un color rojizo cuando se calienta.
El indio se utiliza principalmente para crear aleaciones para usos industriales. Se puede agregar al acero para hacerlo más resistente a la corrosión. También se utiliza para producir aleaciones con estaño, que es útil en electrónica y dispositivos electrónicos. Además, el indio también juega un papel importante en la fabricación de componentes electrónicos.
Además de estos usos industriales, el indio también se utiliza para producir materiales refractarios para aislamiento térmico. También se utiliza en células solares y sensores. Finalmente, se utiliza para producir revestimientos antiadherentes para utensilios de cocina.
El indio tiene un punto de fusión de 156,60 °C y un punto de ebullición de 2072 °C. Tiene una densidad relativa de 7,29 g/cm3 y un estado de oxidación de +3. Su color es blanco grisáceo cuando está puro, pero toma un color rojizo cuando se calienta.
El indio se utiliza principalmente para crear aleaciones para usos industriales. Se puede agregar al acero para hacerlo más resistente a la corrosión. También se utiliza para producir aleaciones con estaño, que es útil en electrónica y dispositivos electrónicos. Además, el indio también juega un papel importante en la fabricación de componentes electrónicos.
Además de estos usos industriales, el indio también se utiliza para producir materiales refractarios para aislamiento térmico. También se utiliza en células solares y sensores. Finalmente, se utiliza para producir revestimientos antiadherentes para utensilios de cocina.
Sintético
Radiactivo
Liquido
Gaseoso
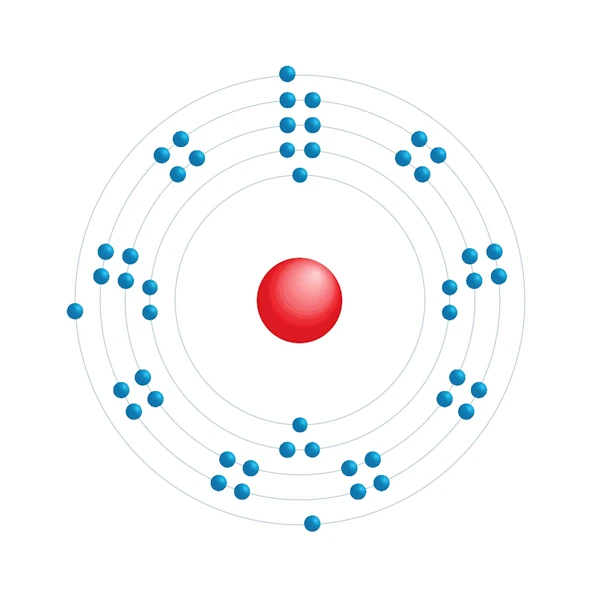
Diagrama de configuración electrónica
| Apellido | indio |
| Número | 49 |
| Atómico | 114.818 |
| Símbolo | In |
| Fusión | 156.2 |
| Hirviendo | 2080 |
| Densidad | 7.31 |
| Período | 5 |
| Grupo | 13 |
| Descubrimiento | 1863 Reich and Richter |
| Abundancia | 0.25 |
| Radio | 2 |
| Electronegatividad | 1.78 |
| Ionización | 5.7864 |
| Número de isótopos | 34 |
| Configuración electrónica | [Kr] 4d10 5s2 5p1 |
| Estados de oxidación | 1,2,3 |
| Electrón por nivel de energía | 2,8,18,18,3 |
| Mineral | Dureza | Densidad |
| Abramovite | ||
| Cadmoindite | ||
| Damiaoite | 5.00 / 5.00 | 10.95 |
| Dzhalindite | 4.00 / 4.50 | 4.34 |
| Indite | 5.00 / 5.00 | 4.67 |
| Indium | 3.50 / 3.50 | 7.20 |
| Ishiharaite | ||
| Kudriavite | 6.58 | |
| Laforêtite | 3.00 / 3.00 | 4.93 |
| Petrukite | 4.50 / 4.50 | 4.61 |
| Roquesite | 3.50 / 4.00 | 4.00 |
| Sakuraiite | 4.00 / 4.00 | 4.00 |
| Yanomamite | 5.50 / 6.00 | 3.87 |
| Yixunite | 6.00 / 6.00 | 18.21 |
| Znamenskyite |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se